Les électrons se comportent comme des ondes
Les physiciens savent depuis longtemps que la lumière est une onde électromagnétique. À ce jour, personne ne doute de cette position, car la lumière montre clairement tous les signes du comportement des ondes : les ondes lumineuses peuvent se chevaucher, générant un motif d'interférence, elles sont également capables de se séparer, en contournant les obstacles le long du temps de diffraction.
Quand nous voyons un oiseau qui marche comme un canard, nage comme un canard et cancane comme un canard, nous appelons cet oiseau un canard. Alors la lumière est onde électromagnétiquesur la base de signes objectivement observés du comportement d'une telle onde dans la lumière.

Cependant, à la fin du XIXe et au XXe siècle, les physiciens vont commencer à parler du « dualisme particule-onde » de la lumière. Il s'avère que la connaissance que la lumière est une onde électromagnétique n'est pas tout ce que la science sait sur la lumière. Les scientifiques ont découvert une caractéristique très intéressante de la lumière.
Il s'avère que la lumière se manifeste d'une manière ou d'une autre COMME le comportement d'un flux de particules d'une manière ou d'une autre.Il a été constaté que l'énergie transportée par la lumière, après avoir été comptée sur une certaine période de temps par un détecteur spécial, s'avère être composée de toute façon de pièces individuelles (entières).
Par conséquent, il est devenu vrai que l'énergie de la lumière est discrète, car elle est composée, pour ainsi dire, de particules individuelles - "quanta", c'est-à-dire des plus petites portions entières d'énergie. Une telle particule de lumière, transportant une unité (ou un quantum) d'énergie, fut appelée un photon.
L'énergie d'un photon se trouve par la formule suivante :
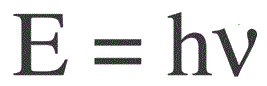
E — énergie des photons, h — constante de Planck, v — fréquence.
Le physicien allemand Max Planck a d'abord établi expérimentalement le fait de la discrétion de l'onde lumineuse et calculé la valeur de la constante h, qui apparaît dans la formule permettant de trouver l'énergie des photons individuels. Cette valeur s'est avérée être : 6,626 * 10-34 J * s. Planck a publié les résultats de ses travaux à la fin des années 1900.

Considérons, par exemple, un rayon violet. La fréquence d'une telle lumière (f ou v) est de 7,5 * 1014 Hz La constante de Planck (h) est de 6,626 * 10-34 J * s. Cela signifie que l'énergie du photon, (E), caractéristique de la couleur violette, est de 5 * 10-19 J. C'est une si petite portion d'énergie qu'elle est très difficile à capter.
Imaginez un ruisseau de montagne - il coule comme une seule unité, et il est impossible de voir à l'œil nu que le ruisseau est en fait composé de molécules d'eau individuelles. Aujourd'hui, cependant, nous savons que l'objet macroscopique - le flux - est en fait discret, c'est-à-dire qu'il se compose de molécules individuelles.
Cela signifie que si nous pouvons placer un compteur de molécules à côté du cours d'eau pour compter les molécules d'eau qui passent au fur et à mesure que le cours d'eau coule, le détecteur ne comptera toujours que des nombres entiers de molécules d'eau, et non des parties partielles.
De même, le graphique de l'énergie totale du photon E, calculé à l'instant t — s'avérera toujours non linéaire (figure jaune), mais pas à pas (figure verte) :
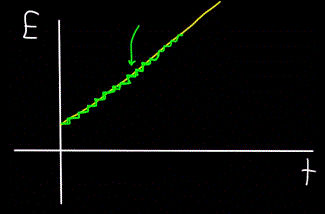
Ainsi, les photons se déplacent, ils transportent de l'énergie, donc ils ont une quantité de mouvement. Mais un photon n'a pas de masse. Comment alors trouver de l'élan ?
En fait, pour des objets se déplaçant à des vitesses proches de la vitesse de la lumière, la formule classique p = mv est tout simplement inapplicable. Pour comprendre comment trouver l'élan dans ce cas inhabituel, tournons-nous vers la relativité restreinte :
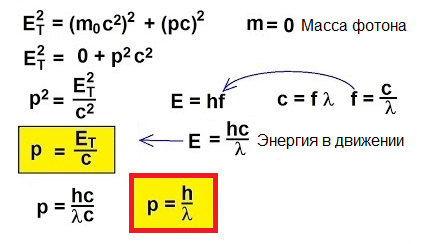
En 1905, Albert Einstein expliquait de ce point de vue effet photoélectrique… Nous savons que la plaque métallique contient des électrons qui, à l'intérieur, sont attirés par les noyaux chargés positivement des atomes et sont donc retenus dans le métal. Mais si vous faites briller une telle plaque avec une lumière d'une CERTAINE fréquence, vous pouvez faire sortir des électrons de la plaque.
C'est comme si la lumière se comportait comme un flux de particules avec une quantité de mouvement. Et même si un photon n'a pas de masse, il interagit toujours d'une manière ou d'une autre avec un électron dans un métal et, dans certaines conditions, un photon est capable d'éliminer un électron.
Donc, si un photon incident sur la plaque a suffisamment d'énergie, alors l'électron sera expulsé du métal et sortira de la plaque avec une vitesse v. Un tel électron assommé est appelé un photoélectron.
Puisque l'électron assommé a une masse connue m, il aura une certaine énergie cinétique mv.
L'énergie du photon, lorsqu'il agit sur le métal, est convertie en énergie de sortie de l'électron du métal (fonction de travail) et en énergie cinétique de l'électron, possédant laquelle l'électron assommé commence à se déplacer hors du métal, le laissant.
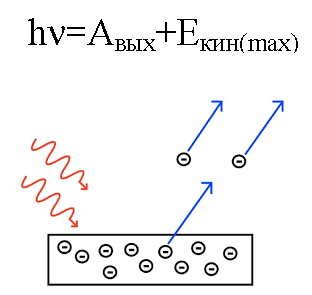
Supposons qu'un photon de longueur d'onde connue frappe la surface d'un métal dont le travail de sortie (d'un électron du métal) est connu. Dans ce cas, l'énergie cinétique d'un électron émis par un métal donné peut facilement être trouvée, ainsi que sa vitesse.
Si l'énergie du photon n'est pas suffisante pour que l'électron remplisse la fonction de travail, l'électron ne peut tout simplement pas quitter la surface du métal donné et le photoélectron ne se forme pas.
En 1924, un physicien français Louis de Broglie proposer une idée révolutionnaire selon laquelle non seulement les photons de lumière, mais les électrons eux-mêmes peuvent se comporter comme des ondes. Le scientifique a même dérivé une formule pour la longueur d'onde hypothétique de l'électron. Ces ondes furent appelées par la suite « ondes de Broglie ».
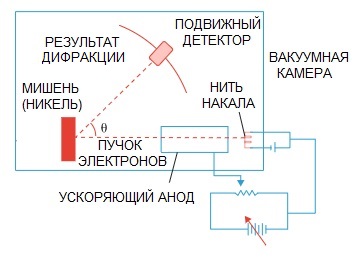
L'hypothèse de De Broglie a été confirmée plus tard. Une expérience de physique sur la diffraction des électrons, menée en 1927 par les scientifiques américains Clinton Davison et Lester Germer, a finalement mis en évidence la nature ondulatoire de l'électron.
Lorsqu'un faisceau d'électrons était dirigé à travers une structure atomique spéciale, il semble que le détecteur aurait dû enregistrer l'image sous forme de particules volant les unes après les autres, ce qui serait logiquement attendu si les électrons étaient des particules.
Mais en pratique on a une image caractéristique de la diffraction des ondes. De plus, les longueurs de ces ondes sont tout à fait cohérentes avec le concept proposé par de Broglie.
En fin de compte, l'idée de de Broglie a permis d'expliquer le principe du modèle atomique de Bohr, et plus tard, elle a permis à Erwin Schrödinger de généraliser ces idées et de jeter les bases de la physique quantique moderne.
