Diélectriques polaires et non polaires
Selon les vues de la physique classique, les diélectriques sont fondamentalement différents des conducteurs, car dans des conditions normales, ils ne contiennent pas de charges électriques libres. La charge totale des particules formant les molécules diélectriques est nulle. Cependant, cela ne signifie pas du tout que les molécules de ces substances ne sont pas capables de présenter des propriétés électriques.
Tous les diélectriques linéaires connus peuvent être divisés en deux grands groupes : les diélectriques polaires et les diélectriques non polaires. Cette division est introduite en raison des différences dans les mécanismes de polarisation des molécules de chaque type de diélectrique. En fait, le mécanisme de polarisation s'avère être un aspect extrêmement important dans l'étude des propriétés physiques et chimiques des diélectriques, et dans l'étude de leurs propriétés électriques.
Diélectriques non polaires
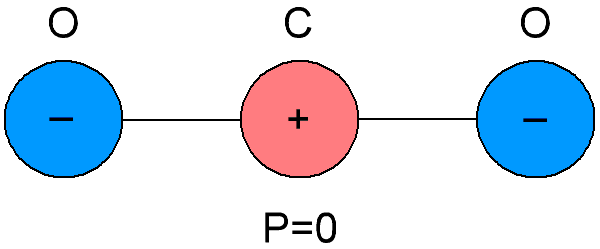
Les diélectriques non polaires sont également appelés diélectriques neutres, car les molécules dont ces diélectriques sont composés diffèrent par la coïncidence des centres de gravité des charges négatives et positives à l'intérieur.En conséquence, il s'avère que les molécules de diélectriques non polaires n'ont pas leur propre moment électrique, il est égal à zéro. Et en l'absence de champ électrique externe, les charges positives et négatives des molécules de ces substances sont disposées symétriquement.
Si un champ électrique externe est appliqué à un diélectrique non polaire, alors la charge positive et négative dans les molécules sera déplacée de leur position d'équilibre d'origine, les molécules deviendront des dipôles dont les moments électriques seront désormais proportionnels à la force de l'électricité champ qui leur est appliqué, et sera dirigé parallèlement au champ.
Des exemples de diélectriques non polaires qui sont utilisés avec succès aujourd'hui comme matériaux isolants électriques sont les suivants : polyéthylène, polystyrène, hydrocarbures, huiles isolantes pétrolières, etc. De plus, les représentants brillants des molécules non polaires sont, par exemple, l'azote, le dioxyde de carbone, le méthane, etc. M.
Les diélectriques non polaires, en raison de leurs faibles valeurs de tangente de perte diélectrique, sont largement utilisés comme diélectriques haute fréquence dans des condensateurs tels que le K78-2.
Diélectriques polaires
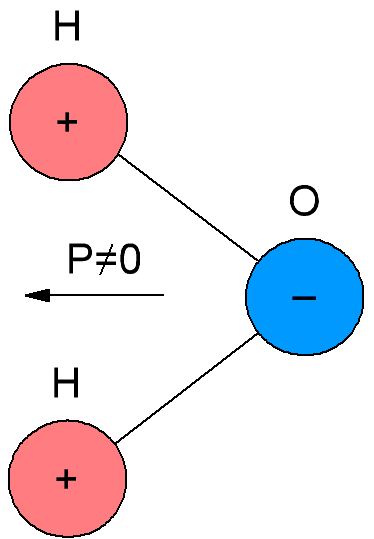
Dans les diélectriques polaires, également appelés diélectriques dipolaires, les molécules ont leur propre moment électrique, c'est-à-dire que leurs molécules sont polaires. La raison en est que les molécules de diélectriques polaires ont une structure asymétrique, de sorte que les centres de masse des charges négatives et positives dans les molécules de ces diélectriques ne coïncident pas.
Si, dans un polymère non polaire, certains des atomes d'hydrogène sont remplacés par des atomes d'autres éléments ou par des radicaux non hydrocarbonés, nous n'obtiendrons qu'un diélectrique polaire (dipôle), car la symétrie sera brisée à la suite d'un tel remplacement. Pour déterminer la polarité d'une substance par sa formule chimique, le chercheur doit bien entendu avoir une idée de la structure spatiale de ses molécules.
Lorsqu'il n'y a pas de champ électrique externe, les axes des dipôles moléculaires sont orientés arbitrairement en raison du mouvement thermique, de sorte qu'à la surface du diélectrique et dans chaque élément de son volume, la charge électrique est en moyenne nulle. Cependant, lorsqu'un diélectrique est introduit dans un champ externe, il se produit une orientation partielle des dipôles moléculaires, de sorte que des charges macroscopiquement connectées non compensées apparaissent à la surface du diélectrique, créant un champ dirigé vers le champ externe.
Des exemples de diélectriques polaires comprennent les suivants : hydrocarbures chlorés, résines époxy et phénol-formaldéhyde, composés de silicium-silicium, etc. Les molécules d'eau et d'alcool, par exemple, sont également des exemples notables de molécules polaires. Les diélectriques polaires sont largement utilisés dans divers domaines technologiques, tels que le piézoélectrique et le ferroélectrique, l'optique, l'optique non linéaire, l'électronique, l'acoustique, etc.

